🫁 Рак лёгкого
Рак лёгкого — это злокачественные эпителиальные опухоли, которые различаются по происхождению, гистологической структуре и клиническому течению.
📊 Эпидемиология
- Наиболее распространённая форма злокачественных опухолей.
- В 2015 году:
- 📌 12% всех злокачественных новообразований в мире.
- 60% случаев зарегистрированы в индустриально развитых странах.
- Заболеваемость (на 100 тыс. населения):
- мужчины — 71,1,
- женщины — 7,7.
- Ежегодно заболевает около 1 млн человек.
🇷🇺 В России (2015 год)
- Ежегодно заболевают 63–65 тыс. человек.
- Стандартизованный показатель на 100 тыс. населения:
- мужчины — 63,6,
- женщины — 7,0.
- Возрастной интервал: 50–65 лет (≈59% случаев).
- Соотношение мужчин и женщин: 8:1.
📈 Причины роста заболеваемости
- Урбанизация и рост числа промышленных предприятий.
- Промышленное загрязнение окружающей среды (профессиональные вредности).
- 🚬 Курение.
🧪 Профессиональные факторы риска
📌 Повышена заболеваемость у рабочих:
- никелевой, алюминиевой и сталелитейной промышленности;
- деревообрабатывающей и металлургической отрасли;
- керамического, асбестоцементного и фосфатного производства.
⚠️ Факторы риска развития рака лёгкого
I. Генетические факторы 🧬
- Перенесённая злокачественная опухоль (ПМЗО).
- ≥3 случаев рака лёгкого у ближайших родственников.
II. Модифицирующие факторы
- Экзогенные:
- курение,
- загрязнение окружающей среды,
- профессиональные вредности.
- Эндогенные:
- возраст >50 лет,
- хронические заболевания лёгких (ХЗЛ):
- пневмония,
- туберкулёз,
- хронический бронхит,
- локальный пневмофиброз,
- заживший инфаркт лёгкого и др.
🔬 Гистологическая классификация рака лёгкого (ВОЗ)
| Группа | Подтипы |
|---|---|
| Плоскоклеточный (эпидермоидный) рак | веретёноклеточный, плоскоклеточный |
| Мелкоклеточный рак | овсяноклеточный, из клеток промежуточного типа, комбинированный овсяноклеточный |
| Железистый рак (аденокарцинома) | ацинарная, папиллярная, бронхоальвеолярный рак, солидный рак с образованием слизи |
| Крупноклеточный рак | гигантоклеточный, светлоклеточный |
| Железисто-плоскоклеточный (диморфный) рак | — |
| Рак бронхиальных желёз | аденокистозный, мукоэпидермоидный, другие типы |
| Другие | редкие формы |
📌 Характеристика основных гистологических типов
1. Плоскоклеточный рак
- Наиболее частая форма — ≈60% случаев.
- Соотношение мужчин и женщин: 15:1.
- > 50% опухолей локализуются центрально (крупные бронхи).
- Чаще встречается у длительно курящих 🚬.
2. Аденокарцинома
- Доля в структуре: 20–26%.
- Встречается чаще у женщин (соотношение 2:1).
- В 80% случаев локализуется в периферических отделах лёгкого.
- Отличается медленным ростом, опухоль может длительно не изменяться в размерах.
3. Бронхиоло-альвеолярный рак (БАР)
- Частота: ≈3,6% случаев.
- Разновидность аденокарциномы.
- Встречается одинаково часто у мужчин и женщин.
- Особенность: аэрогенное метастазирование (распространение по воздухоносным путям).
- Биологические особенности:
- менее злокачественное течение,
- благоприятный прогноз после хирургического лечения,
- mts в регионарные ЛУ на 15% реже,
- 5-летняя выживаемость при I–II стадиях выше на 24%, чем при высокодифференцированной аденокарциноме.
🌍 Международная классификация TNM
| Стадия | T | N | M |
|---|---|---|---|
| 0 | Tis | 0 | 0 |
| IA | T1a, T1b | 0 | 0 |
| IB | T2a | 0 | 0 |
| IIA | T1a, T1b, T2a | 1 | 0 |
| T2b | 0 | — | |
| IIB | T2b | 1 | 0 |
| T3 | 0 | — | |
| IIIA | T1–2 | 2 | 0 |
| T3 | 1–2 | 0 | |
| IIIB | T4 | 2 | 0 |
| Любая T | 3 | 0 | |
| IV | Любая T | Любая N | M1a, M1b |
⚠️ Факторы риска развития
Экзогенные
- 🚬 Курение — основной фактор риска.
- Загрязнение атмосферного воздуха канцерогенами.
- Профессиональные вредности (контакт с канцерогенными веществами).
Эндогенные
- Мужской пол.
- Возраст >50 лет.
- Хронические заболевания лёгких (ХОБЛ, туберкулёз, пневмофиброз и др.).
🏥 Анатомо-клиническая классификация (А. И. Савицкий, 1957)
- Центральная форма:
- эндобронхиальный рак,
- перибронхиальный узловой рак,
- разветвлённый рак.
- Периферическая форма:
- круглая опухоль,
- пневмониеподобный рак,
- рак верхушки лёгкого (Панкоста).
- Атипичные формы:
- медиастинальная,
- костная,
- сердечно-сосудистая,
- печёночная и др.
🩺 Клинические проявления
- Первичные (местные) симптомы
- Связаны с ростом первичной опухоли (стеноз бронха, деструкция, компрессия структур):
- кашель,
- кровохарканье,
- одышка,
- боли в груди.
- Связаны с ростом первичной опухоли (стеноз бронха, деструкция, компрессия структур):
- Вторичные симптомы
- Возникают при:
- метастазах (отдалённых и в лимфатические узлы),
- паранеопластических синдромах.
- Возникают при:
🔬 Гормональная активность опухоли
- В опухоли и плазме выявляются гормонально-активные вещества в высоких концентрациях.
- Радикальное удаление опухоли → нормализация уровня гормонов.
- Удаление гипофиза не снижает уровень гормонов в плазме.
- При эктопической секреции не действует механизм обратной связи (продукция гипофизарных гормонов тормозится).
- При рецидиве или метастазах уровень гормонов снова повышается.
🤒 Паранеопластические синдромы
- Эндокринные:
- Синдром Иценко–Кушинга (АКТГ),
- Гиперпаратиреоз (ПТГ),
- Гинекомастия (ФСГ),
- Остеоартропатия Мари–Бамбергера (СТГ).
- Нейро-кожные и др. синдромы неясного генеза:
- дегенерация мозжечка,
- моторные нарушения,
- полиневрит,
- миопатия,
- дерматомиозит,
- дерматит,
- пузырьковая токсикодермия.
📊 Жалобы и локализация опухоли
| Жалобы / Локализация | Центральная | Периферическая |
|---|---|---|
| Кашель | 68,6% | 66,4% |
| Боли, стеснение в груди | 45,1% | 56,1% |
| Мокрота | 41,6% | 29,0% |
| Слабость | 37,8% | 29,0% |
| Одышка | 26,2% | 20,6% |
| Лихорадка | 19,1% | 5,6% |
| Кровохарканье | 16,5% | 12,1% |
| Похудание, плохой аппетит | 10,8% | 19,6% |
| Без жалоб | 5,2% | 12,1% |
🔬 Диагностика
📋 Обязательные методы исследования
- Общеклиническое обследование.
- Рентгенологические методы:
- рентгенография органов грудной клетки,
- КТ органов грудной клетки → оценка первичной опухоли и регионарных лимфатических узлов.
- Бронхоскопия с забором материала для морфологического исследования:
- отпечатки опухоли,
- смыв с бронхов,
- прямая биопсия,
- транстрахеобронхиальная пункция лимфатических узлов.
- УЗИ: органы брюшной полости, забрюшинное пространство, шейно-надключичные области.
- Радионуклидное исследование скелета.
- КТ головного мозга с контрастированием (исключение метастазов).
- При периферическом раке лёгкого → трансторакальная (чрескожная) пункция опухоли.
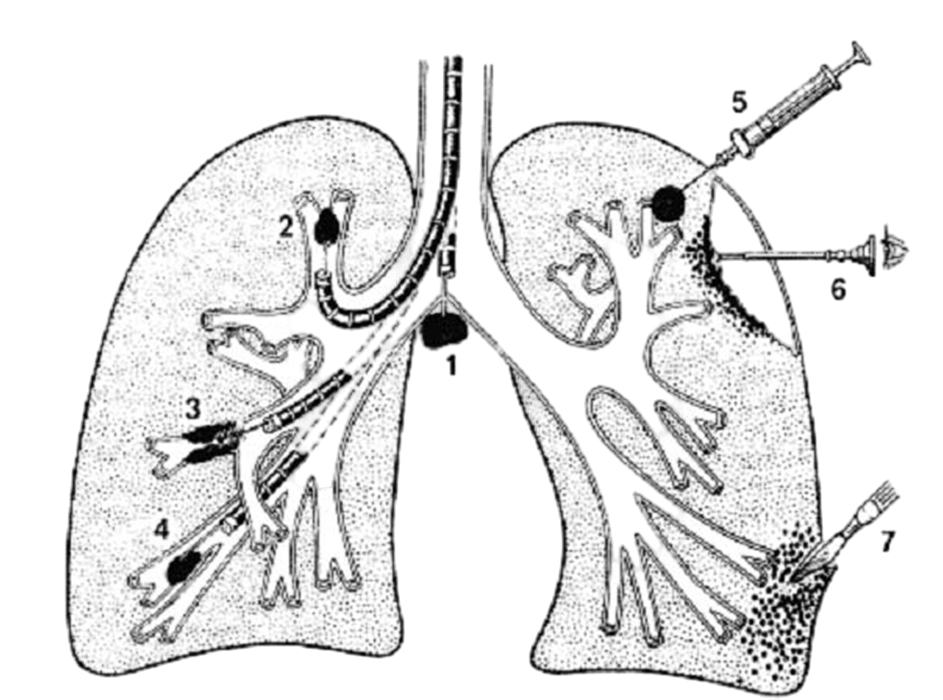
🔬 Методы верификации диагноза
- Диагностическая бронхоскопия.
- Трансторакальная пункция.
- Диагностическая торакоскопия.
- Диагностическая торакотомия.
📌 Трансторакальные аспирационные пункции высокоэффективны при периферических опухолях лёгкого → позволяют верифицировать диагноз в 85,7% случаев (С.А. Величко, 2011).
💉 Трансторакальная пункция
- Наиболее чувствительный метод при периферическом раке лёгкого (выше, чем бронхоскопия).
- Выполняется под контролем КТ.
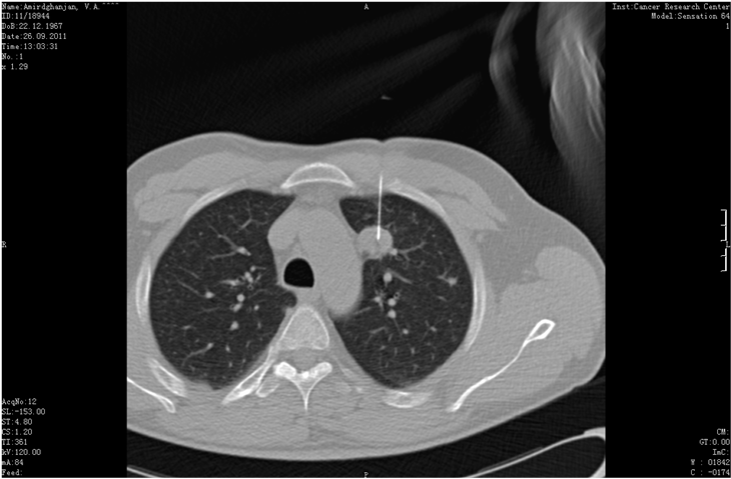
Инструмент
- Игла 18–20 G с внутренним проводником.

❌ Противопоказания
- Нарушения свёртывающей системы крови:
- МНО > 1,3,
- тромбоциты < 50 000/мкл.
- Отсутствие адекватного контакта с пациентом.
- Контралатеральная пневмонэктомия.
- Тяжёлая эмфизема лёгких, не позволяющая выполнить биопсию.
🧭 Схема диагностических исследований
graph TD
node0["Осмотр больного"]
node1["Общеклиническое обследование\nРентгенография\nБронхоскопия\nБиопсия"]
node1["Общеклиническое обследование\nРентгенография\nБронхоскопия\nБиопсия"]
node2["Рак легкого выявлен"]
node3["Рак легкого НЕ выявлен"]
node3["Рак легкого НЕ выявлен"]
node4["Активное наблюдение"]
node2["Рак легкого выявлен"]
node5["Уточнение распространенности опухоли"]
node5["Уточнение распространенности опухоли"]
node6["УЗИ органов брюшной полости и шеи\nКТ головного мозга\nРадиоизотопное исследование\nПЭТ\nМедиастиноскопия\nВидеоторакоскопия\nДиагностическая торакотомия\nМорф. исследование"]
node6["УЗИ органов брюшной полости и шеи\nКТ головного мозга\nРадиоизотопное исследование\nПЭТ\nМедиастиноскопия\nВидеоторакоскопия\nДиагностическая торакотомия\nМорф. исследование"]
node7["Выбор метода лечения"]
node7["Выбор метода лечения"]
node8["Хирургическое\nКомбинированное\nЛекарственное\nЛучевое\nХимио-лучевое\nЭндоскопическое"]
node0 --> node1
node1 --> node2
node1 --> node3
node3 --> node4
node2 --> node5
node5 --> node6
node6 --> node7
node7 --> node8
🔍 Уточнение распространённости опухоли
- УЗИ органов брюшной полости и шеи.
- КТ головного мозга.
- Радиоизотопное исследование (сканирование костей).
- ПЭТ-КТ.
- Пункция (биопсия).
- Медиастиноскопия.
- Видеоторакоскопия.
- Диагностическая торакотомия.
- Морфологическое исследование.
🎯 Выбор метода лечения
- Хирургическое.
- Комбинированное.
- Лекарственное (химиотерапия, таргетная терапия, иммунотерапия).
- Лучевое.
- Химиолучевое.
- Эндоскопическое.
🫁 Лечение рака лёгкого
🔹 Немелкоклеточный рак лёгкого (НМРЛ)
🩺 Хирургическое лечение
- Жизненное показание при НМРЛ.
- Онкологически адекватные операции:
- пневмонэктомия,
- лобэктомия
➝ всегда с систематической медиастинальной ипсилатеральной лимфодиссекцией.
- При необходимости выполняются расширенные операции с резекцией соседних органов:
- грудная стенка, диафрагма,
- верхняя полая вена, лёгочная артерия, аорта и её ветви,
- предсердие, перикард, бифуркация трахеи, пищевод.
☢ Лучевая терапия
- Радикальная программа: СОД ≥ 60 Гр.
- Альтернатива операции — при противопоказаниях или отказе.
- Паллиативная ЛТ: облегчение симптомов.
📌 Лечение по стадиям
| Стадия | Лечение |
|---|---|
| IA | Адъювантная ХТ не показана. |
| IB | Наблюдение или адъювантная ХТ (у <75 лет, группа высокого риска: опухоль >4 см, плевральное вовлечение, сосудистая инвазия, низкая дифференцировка, атипичная резекция, Nх). |
| II–IIIA | Адъювантная ХТ. При невозможности операции — ХЛТ / ЛТ / ХТ. При IIIA (N2) — неоадъювантная ХТ (2 курса) → операция через 3–4 недели. |
| IIIB (местнораспространённый, неоперабельный) | Стандарт — химиолучевая терапия (ХЛТ). Даёт лучшие результаты, чем последовательная терапия, но более токсична. Проводится при ECOG 0–1. |
| IV (метастатический) | Паллиативное лечение ➝ продление жизни, улучшение качества, контроль симптомов. Обязательно раннее начало поддерживающей терапии. |
🧬 Молекулярно-генетическое тестирование
- Обязательный этап выбора терапии.
- При выявлении драйверных мутаций:
- EGFR (экзоны 18–21),
- ALK, ROS1,
- BRAF → назначается таргетная терапия.
- При отсутствии драйверных мутаций ➝ возможна иммунотерапия распространённого НМРЛ.
🔹 Мелкоклеточный рак лёгкого (МРЛ)
- Даже при ранних стадиях: химиотерапия — обязательный компонент.
- При распространённых формах: химиотерапия + лучевая терапия.
- Современные схемы ХТ включают комбинации:
- препараты платины (цисплатин, карбоплатин),
- этопозид,
- гемцитабин (гемзар),
- таксаны (паклитаксел, доцетаксел),
- винорельбин (новельбин).